近期,我院陈忠教授及汪仪研究员团队在Acta Pharmacologica Sinica在线发表了题为“Small-molecule caspase-1 inhibitor CZL80 terminates refractory status epilepticus via inhibition of glutamatergic transmission”的研究论文,首次揭示了课题组前期发现的新型特异性Caspase-1小分子抑制CZL80具有治疗耐药新癫痫持续状态(SE)的作用,并揭示其通过逆转神经炎症介导的兴奋性谷氨酸能突触传递增加而发挥疗效机制。该研究为Caspase-1参与耐药性SE的发病机制提供了实验基础,并为耐药性SE的临床治疗提供潜在药物靶点和新型化合物。

癫痫持续状态(SE)是一种不可预测、严重危及生命的急症,其特点是异常长时间无法自限性终止的癫痫发作。常见以GABAA受体为靶点的一线抗发作药对其治疗有限,且极易在狭窄的治疗窗内产生耐药性。因此,迫切需要深入阐明耐药性SE的发病机制并探寻其治疗的潜在药物靶点。
前期大量研究发现Caspase-1诱导的神经炎症在多种耐药性癫痫中发挥着至关重要的作用。陈忠教授团队前期发现的新型特异性Caspase-1小分子抑制剂CZL80在常见类型的癫痫中具有广谱的抗癫痫活性,还能降低临床耐药性癫痫患者的神经元兴奋性,但是其对于耐药性SE是否具有疗效尚不明确。为此,本研究在前期工作的基础上,利用整体动物耐药性SE模型、药理学干预、基因干预结合在体神经递质释放等手段,深入探究了CZL80对于耐药性SE的作用特征及机制。
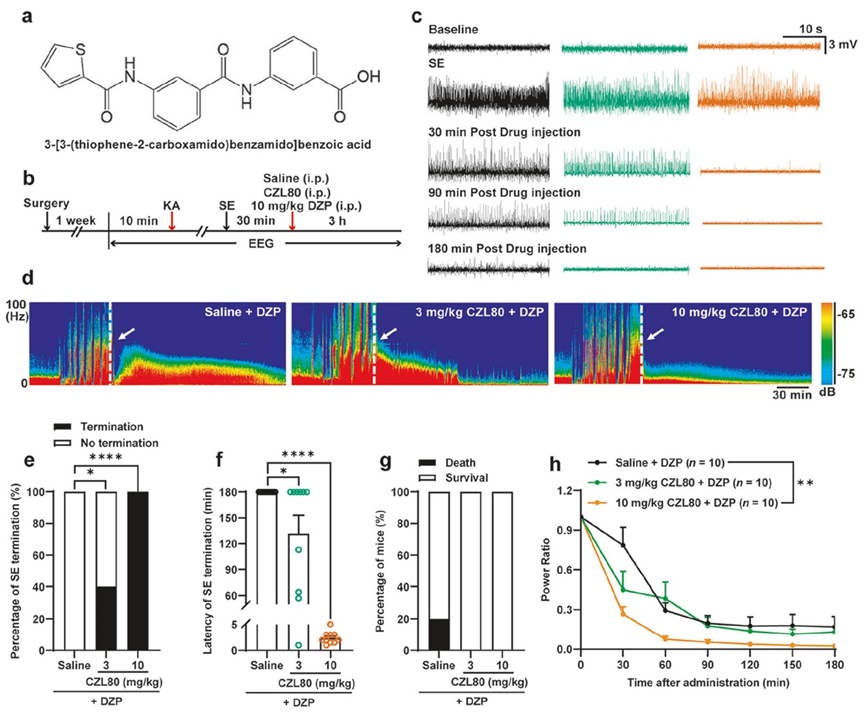
该研究首先建立了经典的小鼠海人藻酸(KA)诱导的SE模型,发现CZL80对SE的治疗潜力,同时显著降低了死亡率。利用联合给药的模式进一步发现CZL80能终止地西泮耐药性SE,并将治疗时间窗延长至3小时,且对SE引起的神经元损伤具有一定的保护作用,为耐药性SE的临床治疗提供了良好的研究基础。
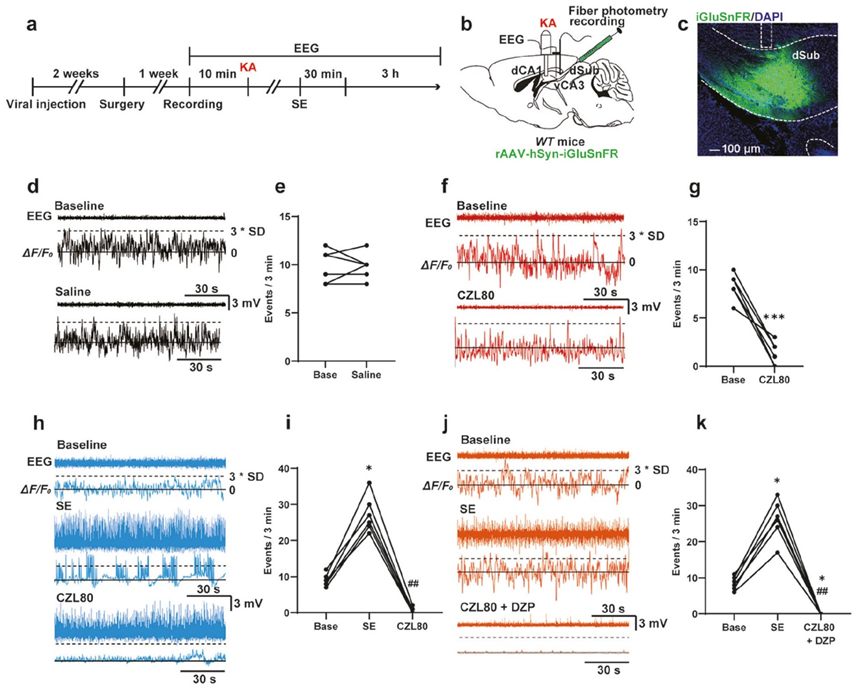
本研究进一步利用Caspase-1-/-和IL1R1-/-转基因敲除小鼠,发现CZL80对耐药性SE的终止作用依赖于caspase-1/IL-1β炎症通路。此外,对癫痫小鼠海马下托谷氨酸神经递质释放进行在体记录验证了CZL80可以抑制神经炎导致的异常增强的谷氨酸能传递。本研究提示Caspase-1是有效治疗耐药性SE的潜在药物靶点,而新型Caspase-1小分子抑制剂CZL80可能是具有抗耐药性SE活性的先导化合物。
该研究的第一作者为我院硕士生王菲,我校第一临床医学院博士后王宇以及我院硕士研究生张擎阳为共同第一作者。陈忠教授和汪仪教授为本文的共同通讯作者。研究也得到了浙江大学永兴集团新入口崔孙良教授的帮助和支持。研究受到了国家国家自然科学基金、浙江省自然科学基金等的资助。
原文链接:
https://www.nature.com/articles/s41401-024-01257-0
团队近照:

浙江省神经药理学与转化研究重点实验室